Батарейка — источник электроэнергии. Как создаётся разность потенциалов?
Как работает батарея и откуда берется напряжение?
Батарея — это химическое, а не механическое устройство. Когда между ее электродами создается замкнутый электрический контур, внутри батареи начинается химическая реакция, которая создает электродвижущую силу, или ЭДС. Именно она обеспечивает разность потенциалов между положительным и отрицательным полюсами.
Если говорить проще, батарея накапливает химическую энергию и преобразует ее в электрическую. Когда к батарее подключают нагрузку, например лампу, прибор или электронную схему, заряд начинает двигаться по замкнутой цепи.
В классическом объяснении направление тока принято считать от положительного полюса к отрицательному. При этом электроны фактически движутся в противоположном направлении — от отрицательного полюса к положительному. Для практической работы с электрическими схемами важно придерживаться одной выбранной системы обозначений и не смешивать эти подходы.
Химическая основа работы батареи
Основой работы батареи является химическая реакция между активными материалами. Обычно это металлы или соединения металлов, а также электролит, который обеспечивает перенос ионов между электродами.
Когда между электродами создается токопроводящий путь, материалы внутри батареи вступают в реакцию. В результате на одном электроде возникает избыток электронов, а на другом — их недостаток. Именно эта разность потенциалов и создает напряжение.
Тип материалов определяет, какое напряжение может создавать один элемент питания. В разных химических системах оно может отличаться: от небольшого напряжения до нескольких вольт на один элемент.
Первые батареи и опыт Вольта
Один из первых примеров электрохимического источника тока создал Алессандро Вольта. Он использовал пластины цинка и серебра, разделенные материалом, смоченным электролитом.
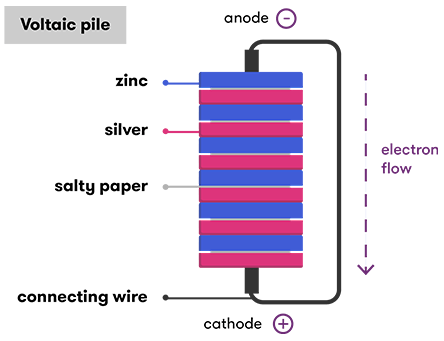
В такой системе возникает окислительно-восстановительная реакция. Во время нее один материал отдает электроны, а другой их принимает. Именно благодаря этому между электродами появляется электрическое напряжение.
Один отдельный электрохимический элемент создает определенное напряжение. Чтобы получить большее напряжение, несколько элементов соединяют последовательно. Именно так работает батарея: она состоит из одного или нескольких элементов питания, объединенных в единую систему.
Почему размер элемента не всегда означает большее напряжение
Напряжение одного элемента зависит прежде всего от химического состава, а не от его физического размера. Более крупный элемент обычно может дольше отдавать ток или работать с большей нагрузкой, но его номинальное напряжение остается определенным химической системой.
Например, если один элемент имеет напряжение около 1,5 В, увеличение его размера не сделает его элементом на 3 В. Для повышения напряжения нужно соединить несколько элементов последовательно.
Поэтому батарею правильнее воспринимать как накопитель химической энергии, который отдает электрическую энергию во время реакции между внутренними материалами.
Что происходит внутри батареи
Внутри батареи постоянно происходят электрохимические процессы. Пока цепь разомкнута, реакция либо почти не происходит, либо идет очень медленно. Когда цепь замыкается, заряд начинает двигаться, и реакция активизируется.
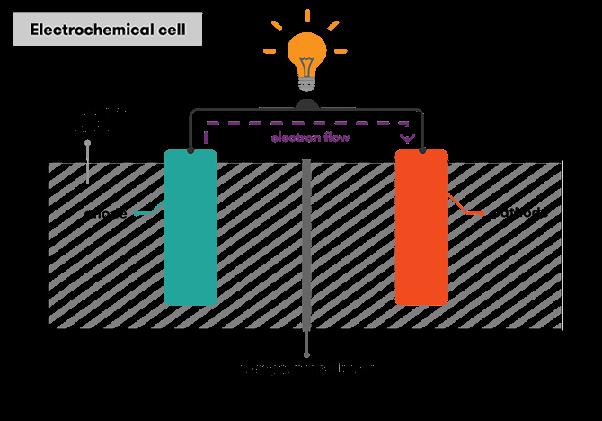
Электролит переносит ионы между электродами, а внешняя цепь обеспечивает движение электронов. Вместе эти процессы создают электрический ток, который питает подключенное устройство.
В реальных батареях процессы могут быть сложнее, чем в базовой схеме. На работу влияют температура, внутреннее сопротивление, качество материалов, состояние электролита и степень разряда.
Направление тока и движение электронов
В технической литературе часто используют понятие обычного тока, который движется от положительного полюса к отрицательному. Это исторически принятое направление, которое применяют в большинстве электрических схем.
Фактическое движение электронов происходит в обратном направлении — от отрицательного полюса к положительному. Оба подхода используются для объяснения электрических процессов, но в практических расчетах важно не смешивать их между собой.
Вывод
Батарея работает благодаря химической реакции между электродами и электролитом. Эта реакция создает разность потенциалов, а после замыкания цепи обеспечивает движение заряда и появление электрического тока.
Напряжение одного элемента зависит от химического состава, а не только от его размера. Чтобы получить большее напряжение, элементы соединяют последовательно. Именно поэтому батарея является не генератором в классическом смысле, а источником накопленной химической энергии, которая преобразуется в электрическую.
Магазин Gtest® — авторизованный поставщик элементов питания в Украину: https://gtest.com.ua/elementy-pitaniya/litievye-batareyki Поставки со склада и под заказ.





